浅谈临床试验项目管理系统的设计和应用
2021-01-28
来源:《中国临床药理学杂志》作者:郝梅,丛翠翠,王瓅珏,张东湖,黄锋,王天兵
摘要: 目的 拟解决临床试验传统纸质管理方式工作效率低、质控难度大及协同管理难等问题。方法 在医院现有信息化基础上,依据国际通用规则、药物临床试验管理规范和医院标准操作规程,设计并搭建了临床试验项目管理系统。结果 该系统已完成一期实施,实现了立项审查、伦理审查、协议审查、试验实施、中心药房管理、结题审查等主要环节的信息化管理。经过 4 年的实际应用,提高了工作效率,提升了服务质量,获得了研究者、申办方、管理部门等的高度认可。结论 临床试验项目管理系统有助于实现临床试验项目统一、规范、专业的管理,为临床试验的顺利实施提供了有力保障。
关键词: 传统纸质管理方式; 临床试验项目管理系统; 效率; 质量
药物临床试验是新药研发过程中的重要环节,对新药的安全性和有效性在上市前进行最后评审起着关键的作用[1]。随着近些年来我院专业组规模的扩大、各专业组的临床研究能力的提升,临床试验项目无论从种类还是数量上都呈逐年快速增长趋势。在药物临床试验机构有限的人力资源条件下,传统的管理模式和手段已经远远无法满足高效率、高质量的管理要求[2]。因此,改进管理模式,积极探索、创新、实践新方法成为一个永恒的话题。本文结合我院临床试验项目管理系统的设计应用及其优势进行阐述,以期为提高医院临床试验质量及管理工作效率,促进试验用药物信息化管理提供思考[3]。
1 现状及存在的问题
目前,国内各机构临床试验药物管理模式主要有机构设立临床试验中心药房统一管理和研究者自行管理两种。主要存在以下 3 个方面的问题。
1. 1 工作效率低
仍然使用各类表格对药物管理过程中的各步骤手工记录,非专业人员多且涉及面广、交接环节多,不熟悉项目、药物管理以及研究者之间的关系[4],导致效率低下。
1. 2 质控难度大
研究者自行管理,试验药物一般由临床专业科室研究护士代为保管,通常采用手工方式,与医院整体药物信息化管理模式不符,且空间有限,安全风险较高,容易造成数据缺失、信息填写不规范或者药物丢失等现象[5],不符合质控管理要求。
1. 3 协同管理难
依靠纸质单据在多个科室和部门间流转,缺乏信息共享,给各临床专业科室和相关部门之间的协调带来困难,且难以追踪溯源。
总之,老式纸质和手工的管理方式所带来的工作效率低下、临床试验质量得不到保障等现象日益严重,利用现有条件,积极开发适用于新药研发的临床试 验 管 理 系 统 ( clinical trial management system,CTMS) ,实施专库、专人管理,是提高药物临床试验质量的重要举措[6 - 7]。
2 系统设计
2. 1 整体架构[8]
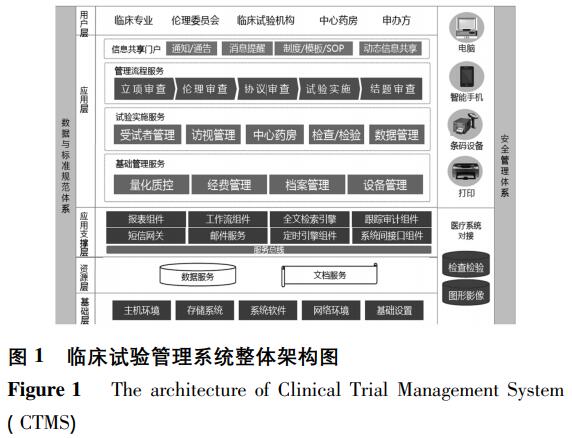
在梳理用户需求的基础上,结合现有技术,进行顶层设计,临床试验项目管理系统的整体架构,见图 1。
CTMS 系统可分 为 两 大 体 系、五 层 结 构,两 大体系是数据与标准规范体系、安 全 管 理 体 系,五层结构分别是指 基 础 层、资 源 层、应 用 支 撑 层、应用层和用户 层。其 中,两 大 体 系 中 数 据 与 标 准 规范体系是系统实现互联互通、信 息 共 享 和 业 务 系统的基 础; 安全管理体系是指安 全管理制度、访问控制 等。五 层 结 构 中,基础层由主机环境、存储系统、系统软件、网络环境和基础设置组成; 资源层提供数据服务和文档服务; 应 用 支 撑 层 主 要提供公共服务,包 括 报 表 组 件、工 作 流 组 件、全 文检索引 擎、跟 踪 审 计 组 件、短 信 网 关、邮 件 服 务、定时引擎组件和系统间接口组件; 应 用 层 主 要 由各主要功能模块组成,包括通知公告、消息提醒等门户网 站,立 项 审 查、伦 理 审 查、协 议 审 查、试 验实施和结题审查等管理流程服务,受试者管理、访视管理、中心药房等试验实施服务,量 化 质 控、经费管理等基础 管 理; 用户层主要为系统的主要使用者,包 括 临 床 专 业、伦 理 委 员 会、临 床 试 验 机构等。
2. 2
免责声明:
1、项目管理信息化网发布的所有资讯与文章是出于为业界传递更多信息之目的,并不意味着赞同其观点或证实其描述。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请浏览者仅作参考,并请自行核实相关内容。
2、本站部分内容转载于其他网站和媒体,版权归原作者或原发布媒体所有。如文章涉及版权等问题,请联系本站,我们将在两个工作日内进行删除或修改处理。敬请谅解!
-
延伸阅读:
-